Jivi® beweist Stärke in vielen Studien
Innovative Zulassungsstudie PROTECT VIII mit über 7-jähriger Extension-Studie
Das Design der PROTECT VIII-Studie reflektiert die gängige Praxis der Einstellung auf eine individuelle Prophylaxedosierung: Die Zuteilung der Patienten in die verschiedenen Behandlungsarme erfolgte auf Basis des klinischen Blutungsprofils der Patienten.1
Studiendesign PROTECT VIII-Haupt und -Extension-Studie:
Hauptstudie:1
- Evaluierung der Sicherheit und Wirksamkeit von Jivi®
- Eingeschlossen wurden Patienten im Alter von 12 bis 65 Jahren mit schwerer Hämophilie A (FVIII < 1 %)
- Untersuchung klar definierter Dosierungsintervalle in den Studienarmen
- Anlehnung an klinische Praxis: Einteilung der Patienten nach Blutungsneigung in 10-wöchiger Run-in-Phase
Extension-Studie:2
- Evaluierung der langfristigen Sicherheit und Wirksamkeit von Jivi®
- Optionale, offene Fortführung der Hauptstudie mit der Möglichkeit die Behandlungsarme zu wechselna,b
- Von 126 Patienten, die die Hauptstudie beendeten, begannen 121 Patienten (96 %) die Extension-Studie
a Ein Wechsel der Behandlungsarme war möglich. Nach Beendigung der Hauptstudie wechselten insgesamt 24 Patienten die Behandlungsfrequenz innerhalb von 7 Tagen nach Beginn der Extension-Studie (1 Patient wechselte vom 2x/Woche-Arm zum 1x/Woche-Arm, 3 Patienten von alle 5 Tage zu 1x/Woche, 7 Patienten von alle 5 Tage zu 2x/Woche, 4 Patienten von 1x/Woche zu 2x/Woche und 9 Patienten von 1x/Woche zu alle 5 Tage).
b Im Arm „variable Frequenz“ sind die Patienten zusammengefasst, die ihre Behandlungsfrequenz nach dem 7. Tag nach Beginn der Extension-Studie hinaus mindestens einmal wechselten.
c 4 Personen brachen die Behandlung während der 10-wöchigen Run-in-Phase ab (1 wegen UE, 3 zogen die Einwilligung zurück).
d Von 126 Patienten, die die Hauptstudie beendeten, begannen 121 Patienten die Extension-Studie.
e Datum Studienende: 21.11.2019. Die Gesamtzeit in der vollständigen Studie (Haupt- und Erweiterungsstudien) betrug 3,9 (0,8-7,0) Jahre
I. E.: Internationale Einheiten; R: Randomisierung; UE: unerwünschtes Ereignis
Jivi®: Individuelle Therapie für Patienten ab 12 Jahre
Langfristig starker Schutz bei einem Injektionsabstand von bis zu 7 Tagen
- Niedrige Blutungsraten in allen Prophylaxe-Armen der PROTECT VIII-Hauptstudie3
- Blutungsraten weiter verringert in der über 7-jährigen Extension-Studie4,5
- Nachhaltiger Blutungsschutz mit fortgeführter Jivi®-Prophylaxe4
a Patienten, die während der Hauptstudie im 1x/Woche-Arm blieben.3,5
b Patienten mit hoher Blutungsneigung: >1 Blutung während der Run-In-Phase (10 Wochen) mit niedriger Dosierung von Jivi® (2x wöchentlich 25 I.E./kg).5
c Patienten mit normaler Blutungsneigung: ≤ 1 Blutung während der Run-In-Phase (10 Wochen) mit niedriger Dosierung von Jivi® (2x wöchentlich 25 I.E./kg).5
d In der Verlängerungsstudie wurden die Patienten nicht nach Blutungsneigung getrennt. Von 134 Patienten, die im Rahmen von PROTECT VIII mit BAY 94-9027 behandelt wurden, schlossen 126 Patienten die Hauptstudie ab, von denen 121 Patienten in die Erweiterungsstudie aufgenommen wurden und in diese Analyse einbezogen sind.4
ABR, Annualisierte Blutungsrate
Stark gegen Blutungen
Wirksame Behandlung mit Jivi®
91% der Blutungen konnten mit ein oder zwei Jivi®-Injektionen gestillt werden.1,a
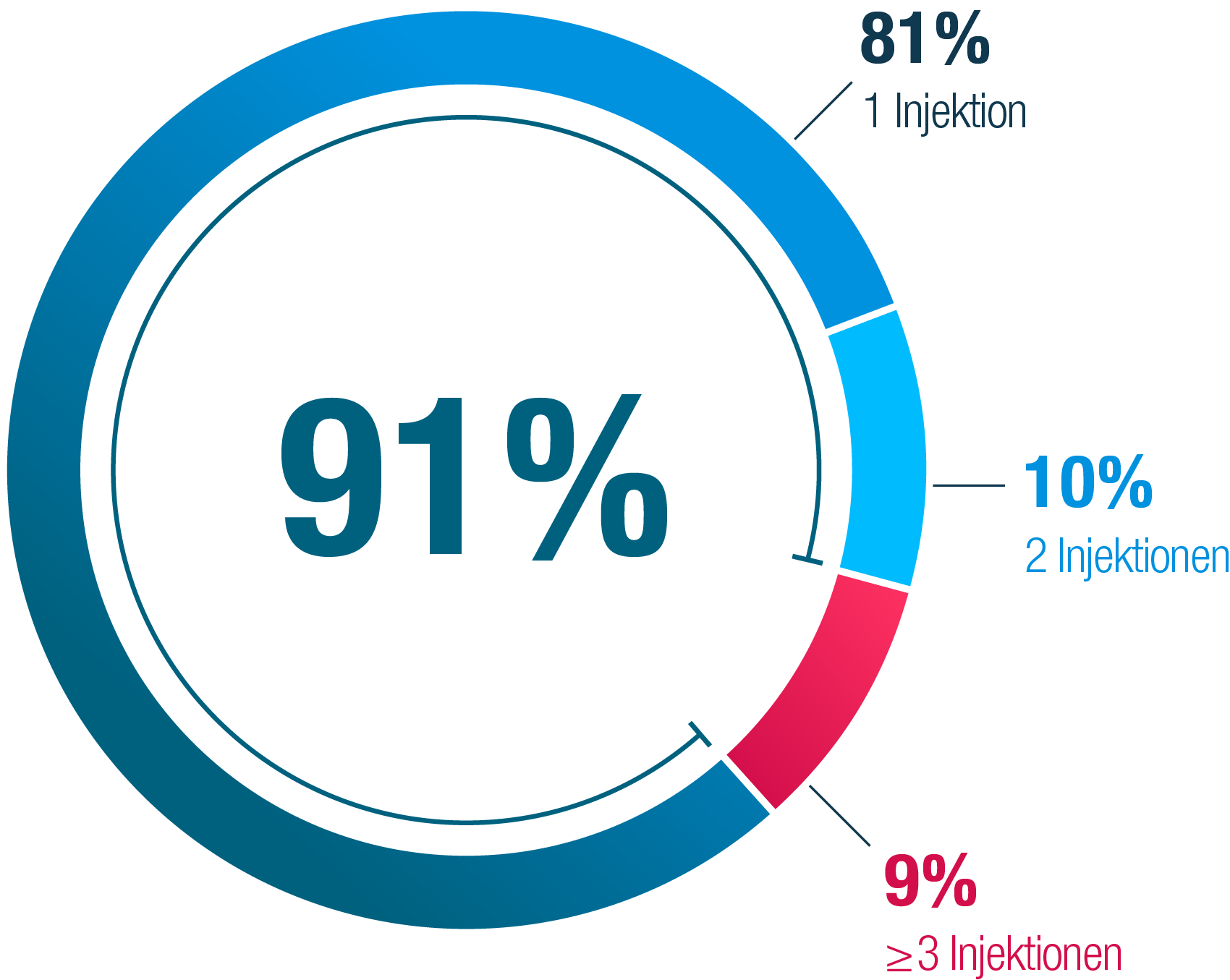
a Bedarfsbehandlung (n=20) und Blutungsbehandlung im Prophylaxeregime (n=112).
1 Reding MT et al. J Thromb Haemost 2017; 15: 411–419
2 Lalezari S et al. Haemophilia 2019; 25(6): 1011-1019
3 Reding MT, et al. J Thromb Haem 2017; 15: 411–419
4 Reding et al. Haemophilia. 2021 May;27(3):e347-e356.
5 Reding MT, et al. Blood 2018; 132(Suppl.1): 1206